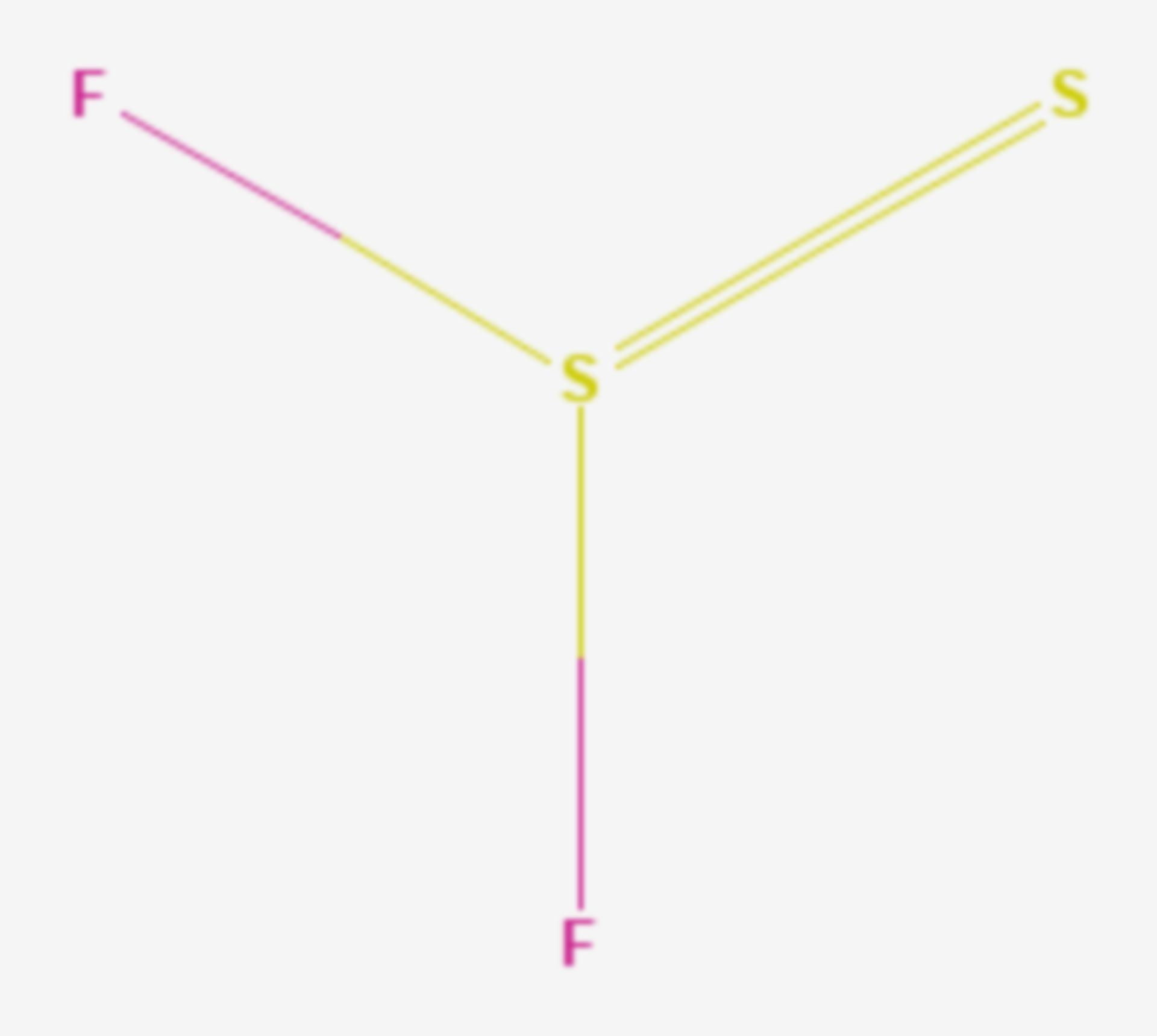
Il cloruro di tiofosforile è un composto inorganico con formula chimica PSCl3. . Si presenta come un liquido incolore dall'odore pungente. Viene sintetizzato dal Tricloruro di fosforo ed è utilizzato per tiofosforilare composti organici nella sintesi di insetticidi.
Sintesi
Il tiofosforil cloruro viene sintetizzato dal tricloruro di fosforo con varie reazioni. La sintesi più comune, usata nella produzione industriale, prevede la reazione diretta del Tricloruro di fosforo con eccesso di zolfo a 180 °C.
- PCl3 S → PSCl3
Con questo metodo la resa, dopo purificazione per distillazione, può essere molto alta. I catalizzatori promuovono la reazione a temperature più basse, ma non sono necessari. In alternativa, la reazione del pentasolfuro di fosforo con il pentacloruro di fosforo conduce al tiofosforil cloruro con resa intorno al 70%.
- 3 PCl5 P2S5 → 5 PSCl3
Reazioni
PSCl3 è solubile in benzene, tetracloruro di carbonio, cloroformio, e solfuro di carbonio. Inoltre, si idrolizza velocemente in soluzioni basiche o idrossiliche, come alcoli o ammine, producendo tiofosfati In acqua PSCl3 reagisce, e produce, a seconda delle condizioni di reazione, acido fosforico, solfuro di idrogeno e acido cloridrico o acido diclorofosforico e acido cloridrico.
- PSCl3 4 H2O → H3PO4 H2S 3 HCl
- PSCl3 H2O → HOP(S)Cl2 HCl
PSCl3 è utilizzato per tiofosforilare (aggiungere il gruppo P=S) i composti organici. Questa reazione è ampiamente utilizzata con ammine e alcoli così come per ammino alcoli, dioli, e diammine. A livello industriale, PSCl3 è utilizzato principalmente per produrre insetticidi come il paratione.
- PSCl3 2 C2H5OH → (C2H5O)2PSCl 2 HCl
- (C2H5O)2PSCl NaOC6H4NO2 → (C2H5O)2PSOC6H4NO2 NaCl
PSCl3 reagisce con le ammidi terziarie per formare tioammidi. Per esempio:
- C6H5C(O)N(CH3)2 PSCl3 → C6H5C(S)N(CH3)2 POCl3
Note
Altri progetti
- Wikimedia Commons contiene immagini o altri file su Cloruro di Tiofosforile